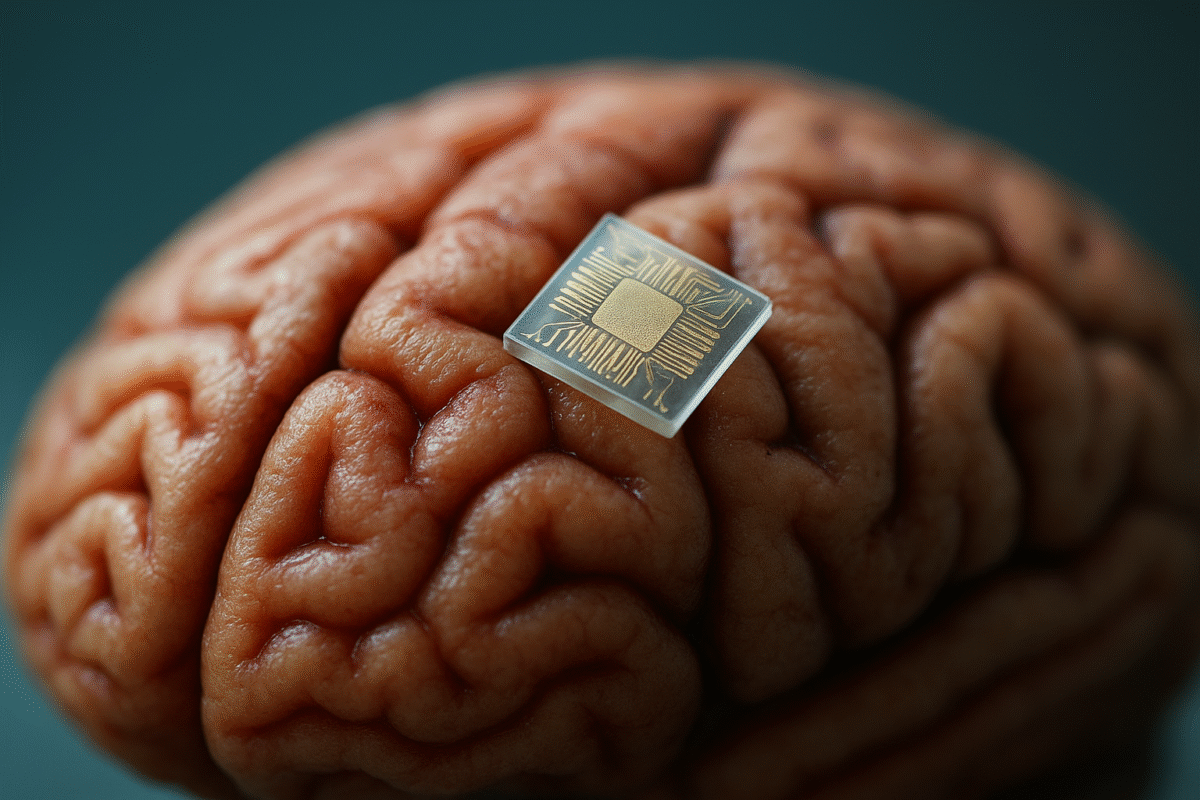
Immaginare di trattare disturbi neurologici complessi con una semplice iniezione non è più solo fantascienza. Un team del MIT Media Lab ha sviluppato minuscoli microchip biocompatibili in grado di viaggiare nel sangue, attraversare la barriera emato-encefalica e auto-impiantarsi in aree specifiche del cervello. Una volta arrivati a destinazione, questi dispositivi possono fornire stimolazioni elettriche mirate, aprendo scenari completamente nuovi per patologie come Alzheimer, depressione, ictus e tumori cerebrali. La tecnologia, battezzata “circulatronica”, punta a superare il limite principale degli impianti tradizionali: la necessità di interventi chirurgici invasivi, costosi e non privi di rischi.
L’idea è di trasformare l’impianto cerebrale da procedura chirurgica unica e complessa a trattamento potenzialmente ripetibile, modulabile nel tempo e gestibile in ambito ambulatoriale. I primi risultati preclinici su modelli animali mostrano che i dispositivi possono inserirsi in regioni cerebrali bersaglio, venire alimentati dall’esterno tramite luce infrarossa e modulare in modo preciso l’attività neuronale circostante, senza danneggiare il tessuto e senza alterare il comportamento degli animali.
Microchip circolanti e “circulatronica”: come funzionano
Nel dettaglio, i ricercatori hanno progettato micro-dispositivi bioelettronici di dimensioni inferiori a una cellula, basati su semiconduttori organici flessibili. Questi microchip sono in grado di convertire la luce infrarossa in energia elettrica, che viene poi sfruttata per stimolare i neuroni del distretto in cui si auto-impiantano. La luce infrarossa, a differenza di altre frequenze, penetra più in profondità nel cranio e nel tessuto cerebrale, permettendo un controllo wireless dal di fuori del corpo.
Il nome “circulatronica” deriva proprio dalla combinazione tra sistema circolatorio ed elettronica: i chip viaggiano nel sangue come se fossero minuscoli satelliti biologici e, una volta raggiunta la zona di infiammazione o di interesse, si fermano e iniziano a funzionare come una rete di micro-elettrodi diffusa. A differenza degli elettrodi tradizionali, che richiedono un posizionamento chirurgico preciso e occupano spazio, qui si parla di milioni di siti potenziali di stimolazione che possono modellare in modo fine l’attività del circuito neuronale.
Il ruolo della barriera emato-encefalica e dei “taxi” cellulari
Uno dei problemi centrali di qualunque terapia diretta al cervello è la barriera emato-encefalica (BEE), una struttura altamente selettiva che blocca la maggior parte delle molecole e protegge il sistema nervoso da tossine e patogeni. Per aggirare questo ostacolo senza aprire chirurgicamente la barriera, il gruppo del MIT ha sfruttato cellule immunitarie specializzate, i monociti, che naturalmente riescono a varcare la BEE quando sono richiamati da zone infiammate.
Attraverso una tecnica nota come “click chemistry”, i ricercatori hanno rivestito sia i monociti sia le superfici dei microchip con gruppi chimici complementari, creando una sorta di “velcro molecolare”. In questo modo, le cellule diventano veicoli che trasportano l’elettronica all’interno del cervello: un autentico “cavallo di Troia” cellulare che consente di attraversare la barriera senza danneggiarla, mantenendo intatta la sua funzione protettiva.
Microchip e stimolazione cerebrale mirata: risultati nei modelli animali
Nei primi esperimenti su topi, i ricercatori hanno indotto una condizione di infiammazione cerebrale per simulare uno scenario patologico realistico. Dopo l’iniezione nel flusso sanguigno, i microchip legati ai monociti hanno seguito il richiamo infiammatorio e si sono auto-impiantati proprio nelle aree coinvolte. Successivamente, un fascio di luce infrarossa proveniente dall’esterno del cranio ha alimentato i dispositivi, che hanno prodotto impulsi elettrici in grado di modulare l’attività neuronale nella regione bersaglio.
Le analisi hanno mostrato che la stimolazione è localizzata e precisa, nel raggio di pochi micron dall’impianto, con un impatto minimo sul tessuto circostante. I topi non hanno evidenziato alterazioni misurabili nel comportamento o nei parametri vitali, indicando un buon profilo di sicurezza a breve termine. Si tratta di risultati ancora preliminari, ma sufficienti a suggerire che la circulatronica possa rappresentare una piattaforma concreta per future terapie umane.
Dalle malattie infiammatorie alle patologie degenerative
Sebbene i test iniziali si siano concentrati sull’infiammazione, il potenziale d’uso è molto più ampio. In prospettiva, lo stesso principio potrebbe essere applicato a malattie neurodegenerative come Alzheimer, a disturbi psichiatrici resistenti ai farmaci, a forme di epilessia focale e persino a determinati tumori cerebrali. In questi casi, una rete di impianti auto-distribuiti potrebbe fornire neuromodulazioni mirate o combinarsi con altre strategie terapeutiche, come farmaci o immunoterapie.
Alcuni tipi di tumore o lesione si estendono in regioni profonde o difficili da raggiungere con la chirurgia tradizionale; poter inviare dispositivi attraverso i vasi sanguigni ridurrebbe drasticamente la complessità dell’intervento e potrebbe offrire opzioni a pazienti considerati inoperabili.
Verso i primi test sull’uomo: prospettive e sfide
Il team guidato da Deblina Sarkar, come riportato anche nell’ articolo di MIT News dedicato ai nuovi impianti cerebrali senza chirurgia , è al lavoro per portare questa tecnologia dal laboratorio alla clinica. Attraverso la startup Cahira Technologies, l’obiettivo è avviare i primi studi clinici nell’arco di pochi anni, iniziando da condizioni neurologiche in cui le opzioni terapeutiche sono limitate e il bisogno di alternative è più urgente.
Le sfide da affrontare non mancano: dimostrare la sicurezza a lungo termine, garantire che i dispositivi non interferiscano con funzioni cognitive complesse, definire protocolli di somministrazione e di stimolazione adatti a pazienti molto diversi tra loro. Sarà necessario anche ottimizzare la produzione su larga scala dei microchip, renderne tracciabile il percorso all’interno del corpo e sviluppare interfacce cliniche user-friendly per medici e centri ospedalieri.
Cosa potrebbe cambiare per i pazienti
Se la tecnologia manterrà le promesse, i futuri pazienti potrebbero beneficiare di trattamenti personalizzati basati su una combinazione di iniezioni periodiche di dispositivi, sessioni di stimolazione programmata e monitoraggio non invasivo dell’attività cerebrale. La circolazione sanguigna diventerebbe una sorta di “autostrada terapeutica”, lungo la quale micro-sistemi intelligenti vengono trasportati esattamente dove servono, quando servono.
L’idea di usare microchip sub-cellulari come alleati silenziosi, integrati con cellule del sistema immunitario e comandati da fasci di luce, ridisegna il confine tra elettronica, biologia e medicina. Non si parla più solo di impianti nel cervello, ma di una vera e propria simbiosi tra tessuto nervoso e dispositivi programmabili, con l’obiettivo di intervenire sui circuiti malati lasciando intatti quelli sani.